ESMO-Asia | 君赛生物GC101 TIL治疗后线黑色素瘤RCT临床亮相
2025年12月5-7日,欧洲肿瘤内科学会亚洲年会(ESMO-Asia)将于新加坡盛大举行,该活动是聚焦全球肿瘤诊疗领域的顶级国际学术盛会,旨在汇聚全球顶尖专家,重点关注亚太地区的肿瘤发病特点,分享肿瘤领域前沿新技术与诊疗进展,推动国际学术交流与合作。
这一新研究方案将以壁报和线上的形式,与业界专家同步分享。
壁报概要

摘要编号 :#818TiP
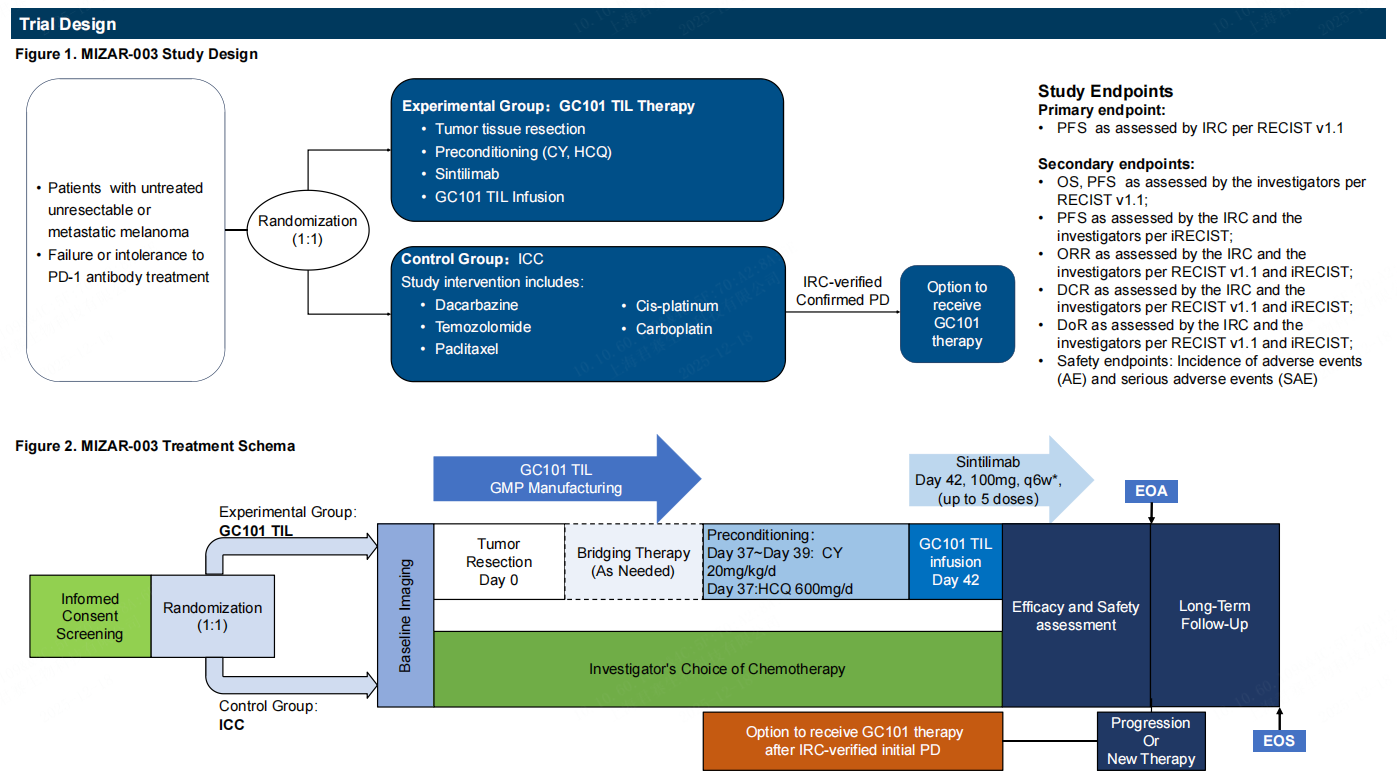
摘要题目:Trial in progress: A Pivotal Phase 2, Randomized, Controlled, Open-Label, Trial (MIZAR-003) to Assess the Efficacy and Safety of GC101 TIL, an Autologous Tumor-Infiltrating Lymphocyte (TIL) Cell Therapy, for Patients with Advanced Anti-PD-1 Refractory Melanoma in Later-Line Therapy
主要研究者:郭军教授
主要研究机构:北京大学肿瘤医院
展示时间:2025.12.5-12.7全程
(正式壁报12月5日起可于君赛生物官网查看:https://www.juncell.com/academic-achievements)
研究背景
免疫检查点抑制剂(ICIs)与靶向治疗虽彻底改变了晚期(不可切除或转移性)黑色素瘤的治疗格局,但临床仍面临巨大挑战:大多数接受一线ICIs治疗的患者在一年内会出现疾病进展[1-3],且40%-65%患者存在原发性耐药,30%-40%患者会发生继发性耐药[4-6]。
TIL疗法对ICIs治疗失败的晚期黑色素瘤患者已显示出具有临床意义的疗效[7,8],但其应用受限于治疗相关毒性——传统治疗方案需高强度清淋预处理(高剂量环磷酰胺+氟达拉滨),同时联合大剂量IL-2,不良反应突出。
君赛生物针对常规TIL疗法的核心痛点问题,开发出了无需高强度清淋化疗,无需IL-2给药的GC101 TIL疗法,该方案在前期Ⅰ期临床试验中已显示出优异的疗效与安全性[9]。
▼ 案例回看

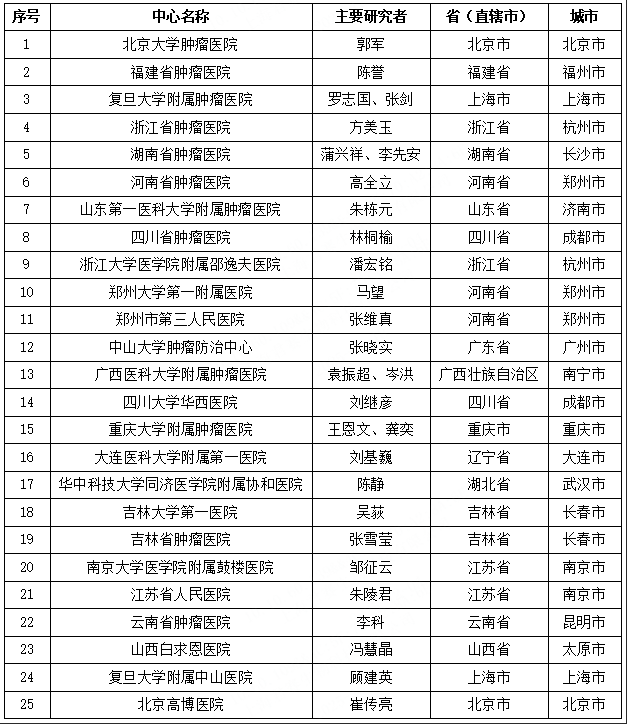
▼ MIZAR-003临床试验中心

声明:
本文内容仅作为信息分享和观点展示,旨在传递前沿专业信息和满足医疗专业人士的信息需求,无意做任何产品的推广或治疗方案推荐。本文所涉GC101处于临床试验阶段,尚未获批上市。任何关于疾病的诊断和治疗等医疗行为,请遵从医疗卫生专业人士的指导。

君赛生物专注于TIL疗法开发,自主建立国际领先的DeepTIL™细胞富集扩增与NovaGMP™基因修饰技术平台,据此开发一系列全球领先的TIL创新疗法,其中2款已进入临床试验阶段,正面向社会招募晚期实体肿瘤患者。
处于关键II期临床的全球首款无需高强度清淋化疗,无需IL-2给药的天然TIL疗法GC101,以及处于临床I期的全球首创的非病毒载体基因修饰TIL疗法GC203,在10余种不同类型晚期实体肿瘤中均展现优异临床疗效(包括多线治疗失败的胰腺癌与高级别脑胶质瘤),多例患者肿瘤被完全清除,且维持无瘤生存最久已超4年。
君赛生物将坚守“精雕细胞,守望生命”的崇高使命,胸怀“以科技创奇迹,使奇迹变平常”的美好愿景,秉承“专注、拓新、包容、共享”的核心价值观,使高临床价值的创新 TIL 疗法惠及更多癌症患者。
更多信息请访问:www.juncell.com